+ محدودیت زمان: ۱ ثانیه
+ محدودیت حافظه: ۲۵۶ مگابایت
----------
از شما میخواهیم برنامهای بنویسید تا با دریافت نام عناصر، [آرایش الکترونی](https://fa.wikipedia.org/wiki/%D8%A2%D8%B1%D8%A7%DB%8C%D8%B4_%D8%A7%D9%84%DA%A9%D8%AA%D8%B1%D9%88%D9%86%DB%8C) آن را نشان دهد.
طبق این نظریه، الکترونها در تعدادی «لایه» قرار دارند، هر «لایه» از تعدادی «زیرلایه» تشکیل شده که هر کدام ظرفیت تعدادی الکترون دارند. ۴ نوع زیرلایه داریم که با حروف `s`، `p`، `d` و `f` نشان میدهیم. ظرفیت این لایهها بهترتیب ۲، ۶، ۱۰ و ۱۴ الکترون است. هر «لایه»، از تعدادی «زیرلایه» تشکیل شده:
+ لایهی اول ($n = 1$). یک زیرلایهی `s`.
+ لایهی دوم ($n = 2$). یک زیرلایهی `s` و یک زیرلایهی `p`.
+ لایهی سوم ($n = 3$). یک زیرلایهی `s`، یک زیرلایهی `p` و یک زیرلایهی `d`.
+ لایهی چهارم به بعد ($n \ge 3$). یک زیرلایهی `s`، یک زیرلایهی `p`، یک زیرلایهی `d` و یک زیرلایهی `f`.
حال میتوانیم لایه و زیرلایهها را به صورت یک رشته با دو کاراکتر نشان دهیم. مثلاً `3p` یعنی زیرلایهی نوع `p` در لایهی سوم.
اگر یک اتم از $e$ الکترون تشکیل شده باشد به ترتیب زیر، یکی یکی به زیرلایهها اضافه میشود تا ظرفیت آن پر شود و سپس به سراغ زیرلایهی بعدی میرود.
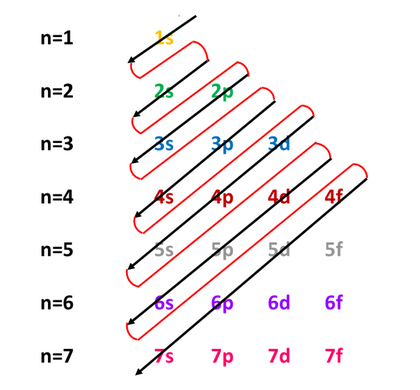
در این اتمهای `Cu`، `Cr`، `Nb`، `Mo`، `Ru`، `Rh`، `Pd`، `Ag`، `La`، `Ce`، `Gd`، `Pt`،
`Au`، `Ac`، `Th`، `Pa`، `U`، `Np`، `Cm` و `Lr`
استثنا هستند و از قوانین گفته شده پیروی نمیکنند. میتوانید آرایش الکترونی آنها را از [اینجا](https://chem.libretexts.org/Ancillary_Materials/Reference/Reference_Tables/Atomic_and_Molecular_Properties/A1:_Atomic_Electron_Configurations) مشاهده کنید.
# ورودی
در سطر اول ورودی، عدد صحیح $t$ داده میشود.
$$1 \leq t \leq 10$$
در $t$ سطر بعدی، در هر سطر، نام یک عنصر به صورت یک رشته از حروف کوچک و بزرگ انگلیسی است که حرف اول بزرگ و سایر حرفها کوچک است داده میشود.تضمین میشود نام این عنصر در ۱۰۴ عنصر اول جدول تناوبی موجود باشد.
# خروجی
خروجی $t$ سطر دارد و در هر سطر، زیرلایههای اتم را مانند نمونهها چاپ کنید.
# مثال
## ورودی نمونه ۱
```
2
Mg
Cu
```
## خروجی نمونه ۱
```
1s2 2s2 2p6 3s2
1s2 2s2 2p6 3s2 3p6 3d10 4s1
```